Neue Hoffnung im Kampf gegen Viren und Krebszellen
Nach Ausbruch der SARS-CoV-2-Pandemie wurde eine geniale Idee für die Entwicklung eines Impfstoffs aufgegriffen: Die Rolle der messengerRNA zur Aktivierung des Immunsystems gegen das Virus. Seitdem ist die Biochemie und vor allem die weitere Erforschung der RNA sowie der vielen Vorgänge im Energiestoffwechsel der Zelle ein boomender Bereich. Besonders für die Krebsbekämpfung verspricht dieser Forschungsbereich große Fortschritte.
Unsere Körperzellen sind wie ein lebender Maschinenraum. Sie sind wie winzige Kraftwerke, in denen es keine Schichtarbeit, keine Pausen, keinen Feiertag oder gar Urlaub gibt; hier wird ohne Unterbrechung 24 Stunden am Tag geschuftet! Und das ist auch gut so: Das ist die Voraussetzung für Leben.
In den Zellen findet der Energiestoffwechsel und vor allem die Proteinbiosynthese statt – die lange Zeit unterschätzte faszinierende Tätigkeit der Ribonukleinsäure (RNA oder Ribonuclein Acid). Mit der Entwicklung von Impfstoffen gegen das aktuelle SARS-CoV-2 Virus ist die Rolle der Ribonukleinsäure zu einem heißen Thema geworden. Dahinter stand die Idee, die körpereigenen Erneuerungs-, Reparatur- und Verbesserungsprozesse der Proteinbiosynthese, insbesondere einen dabei kurzfristig aktiven Teil der RNA – der Boten-RNA oder mRNA – zu benutzen, um eine Virusinfektion zu bekämpfen. In diesem Fall wird die synthetisch hergestellte mRNA mit einer besonderen Information ausgestattet: der eines kleinen Proteinteilchens des Virus (oder auch einer Krebszelle), mit dem die Krankheit bekämpft werden soll. Mit dieser Information wird unser Immunsystem „gereizt“, da diese Proteinteilchen unbekannt sind und eine sofortige Abwehrreaktion einsetzt. Solange also das eingeimpfte mRNA-Nukleid die kleinen Fremdkörper vermehrt, ist unser Immunsystem hochaktiv. Auf diese Weise funktioniert die Impfung: Von nun an sind unser Immunsystem und damit alle unsere Zellen vorgewarnt, wenn ein entsprechendes Virus (oder eine Krebszelle) eindringen will. Diese kommen gar nicht erst dazu, sich zu vermehren, da sie sofort ausgeschaltet werden – so als würde jemand auf den „Aus“-Schalter drücken.
Diese geniale Idee ist bereits fast 40 Jahre alt und war ursprünglich als Methode zur Bekämpfung von Krebszellen und Metastasen gedacht. Allerdings fristete dieser Ansatz seither ein Schattendasein. Erst mit der Covid-Pandemie und der möglichst schnellen Entwicklung von Impfstoffen wurde dieser faszinierende Bereich der Forschung wieder aufgegriffen.

Eine der ersten, die sich schon in den 1980er Jahren mit der Entwicklung von mRNA-Therapien beschäftigt hat, ist die ungarische Biochemikerin Dr. Katalin Karikó. Allerdings begann die ursprüngliche Idee dieser Forschung mit einem ganz anderen Ziel, nämlich der Bekämpfung von Krebs.
Katalin Karikó hat sich ganz der Forschung mit der sogenannten „Boten-RNA“ oder messengerRNA verschrieben und hat nach 40 Jahren unbeirrter Forschung einen Weg für die Herstellung eines Impfstoffes auf der Basis der mRNA-Prozesse in unseren Zellen gefunden. Ihre wissenschaftliche Karriere begann in ihrer Heimat Ungarn an der Universität Szeged, wo sie damals bereits die Ribonukleinsäure (RNA) synthetisieren konnte. Doch nach ihrer Post-doc-Zeit am Biological Research Centre der Ungarischen Akademie der Wissenschaften war sie im Jahre 1985 gezwungen, mit Ehemann und Kind und einem Startkapital von gerade einmal 900 Dollar Ungarn zu verlassen und ins Asyl zu gehen.
Seit 1998 forschte Karikó gezielt an der Entwicklung von Medikamenten auf mRNA-Basis, was in den 90er Jahren jedoch noch ziemliches Neuland war, und kaum jemand bemerkte, daß es sich hier um eine bahnbrechende Idee handelte, die große Hoffnung für die gesamte Medizin darstellen würde. Sie hatte die Idee, daß man durch das Einbringen von künstlich hergestellter mRNA in die Zellen von Patienten diese zur Bildung mangelnder Enzyme, von Wachstumsfaktoren zur Reparatur geschädigten Gewebes oder von Antigenen zur Auslösung von Immunreaktionen anregen kann.
Nach langen, vergeblichen Versuchen, Forschungsgelder für ihre Idee aufzutreiben und nach mehreren Rückschlägen schaffte sie es schließlich, virale RNA-Moleküle durch eine gezielte Veränderung eines der vier Bausteine so zu modifizieren, daß diese in der Zelle nicht mehr von der Immunabwehr eliminiert wurden. Angesichts der Dringlichkeit, schnell einen funktionierenden Impfstoff gegen Covid-19 zu entwickeln, griffen verschiedene Forschungsinstitute wieder auf diese mRNA-Idee zurück. Auf einmal waren genug Gelder da, und der Schritt in eine große Zukunft der Medizin – der biochemischen Medizin – begann. Seit 2013 ist Katalin Karikó Senior Vice President des deutschen Biotechnologieunternehmens BioNTech RNA Pharmaceuticals AG.
Die spannende Arbeit mit RNA
Was die DNA ist und daß sie unser Erbgut im Zellkern speichert, haben wir alle im Biologieunterricht gelernt, denn es ist eine spannende Frage, wo sich die eigenen Geninformationen befinden. Doch im Grunde fragen wir uns eher, wie sich denn diese Geninformationen jeden Tag – oder besser jederzeit – mit unserer Nahrung im ganzen Körper verteilen, d.h. wie weiß unsere Leber oder unsere Nasenspitze, welcher Teil vom eben verspeisten Wurstbrötchen jetzt zu ihrer Verfügung steht? Und ob das Wurstbrötchen überhaupt als nützliche Nahrung von den Zellen erkannt wird, und wie das Wurstbrötchen eigentlich bis in unsere Zellen kommt.
Hier fängt die besondere Rolle der RNA (Ribonukleinsäure) an, die sich zusammen mit der DNA in unseren Zellen befindet. Ein riesiges Gebiet der biochemischen Forschung hat sich eröffnet, um herauszufinden, wie unser Wurstbrötchen in einem höchst komplizierten Prozeß bis in die kleinsten Mikroteilchen zerlegt wird und wie die RNA es schafft, der Leber, den Hautzellen, den Muskeln und Nervenzellen genau die „Nahrung“ zukommen zu lassen, die sie für Reparatur, Aufbau und alle Lebensfunktionen brauchen. Eigentlich ist es eher ein Molekülcocktail, der nach einem langen Weg über das Blut am Ende in unseren Zellen ankommt und der dann von der RNA – nicht der DNA! – mit dem richtigen „Gencode“ versehen wird. Die im Gegensatz zur Doppelhelix der (zweisträngigen) DNA nur einsträngigen RNA-Moleküle speichern während des komplizierten Vorgangs nicht nur den genetischen Code, sie entfalten sich auch in einzelne Teile und wirken dann wie Enzyme und Katalysatoren. Dieser Vorgang nennt sich Proteinbiosynthese.
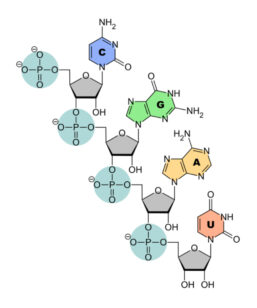
Die Bausteine der DNA (Desoxyribonukleinsäure) und der RNA (Ribonukleinsäure) bestehen aus immer den gleichen Basen Adenin, Guanin, Cytosin und Thymin; bei der RNA wird das Thymin durch Uracil ersetzt. Sie sind durch das Zuckermolekül Ribose (bei der RNA) bzw. Desoxyribose (bei der DNA) und einem Phosphat miteinander verknüpft (Abbildung 1). Die Stränge bestehen also aus Nukleinbasen, Zuckern und löslichem Phosphat. Die jeweils vier Basen treten aber nicht nur als Monophosphate (NMP) verknüpft in den informationstragenden Makromolekülen von Nukleinsäuren auf, also z.B. als Adenosinmonophosphat, sondern sie haben daneben noch verschiedene weitere Funktionen für die Regulation von Lebensvorgängen in der Zelle selbst und spielen als Triphosphate wie Adenosintriphosphat (ATP) oder Guanosintriphosphat eine zentrale Rolle beim Energietransfer bei den Stoffwechselvorgängen in der Zelle, praktisch wie Katalysatoren bei der Proteinbiosynthese. Das heißt, sie sind Antreiber bzw. Initiatoren von Prozessen. Zum Beispiel spielen sie eine zentrale Rolle bei den Enzymaktivitäten der Proteinbiosynthese und wohl auch beim Transport von Enzymen.
Der Zucker Ribose der Ribonukleinsäure besitzt ein Sauerstoffatom mehr als die Desoxyribose (daher der Name DNA). Dadurch ist die RNA vergleichsweise sehr instabil, aber auch chemisch viel aktiver als das DNA-Molekül. Außerdem ist die DNA immer ein Doppelstrang aus den vier miteinander verknüpften Basen, die RNA dagegen immer ein Einzelstrang (siehe Abbildung 2). Auch die Längen der einzelnen RNA-Moleküle sind sehr unterschiedlich. Beispielsweise sind die transfer-RNAs immer sehr klein, sie haben ungefähr die Länge von ca. 80 Nukleotiden. Daneben gibt es die mRNA (Boten-RNA) und noch einige andere micro-RNAs, die alle an der Proteinbiosynthese sowie der Transkription und Translation der Proteine beteiligt sind. Alle diese RNA-Arten sind in der Zelle fünf- bis zehnmal häufiger als die DNA; sie stellen daher den größten Teil der Nukleinsäuren in der Zelle dar.

Die Entdeckung des Energiestoffwechsels der Zelle
Die Bedeutung des Phosphatstoffwechsels und die entscheidende Rolle des Adenosintriphosphats (ATP) als operativer Substanz in der Zelle sowie die Einzelschritte der Glykolyse wurden erst 1930 von Otto Meyerhof und Karl Lohmann in Heidelberg entdeckt, wodurch praktisch eine neue Ära der Zellforschung und vor allem der Aufklärung des Energiestoffwechsels der Zelle begann. Diese sogenannte „Zellatmung“ besteht aus Stoffwechselvorgängen, bei denen Glukose (also Zucker) abgebaut und ATP produziert wird. Diese Erkenntnisse revolutionierten die Erforschung der Stoffwechselprozesse in der Zelle. Meyerhof geriet jedoch schon 1935 unter den Druck der Nationalsozialisten, ihm wurde die Lehrbefugnis entzogen, und 1938 mußte er Deutschland verlassen. Doch Meyerhofs früherer Schüler, der spanische Physiologe und Biochemiker Severo Ochoa (1905–1993) setzte die Forschungsarbeiten zur Proteinsynthese und der Reproduzierung der RNA bis zu seiner Rückkehr nach Spanien fort. Er entdeckte die RNA-Polymerase, dasjenige Enzym, das bei der Proteinsynthese das Ablesen des genetischen Codes in Gang setzt. Später wirkte er an der Entschlüsselung des genetischen Codes mit.
In der Heidelberger Zeit publizierten Meyerhof und seine Assistenten über 250 Originalartikel, die eine zentrale Rolle in der monumentalen Aufgabe spielten, das Riesenpuzzle der Glykolyse zusammenzusetzen. Dies war Beginn und zugleich Höhepunkt der Aufklärung des intermediären Stoffwechsels. In Meyerhofs Institut wurde nicht nur ein Großteil der Substanzen gefunden, die in der Glykolyse eine Rolle spielen; es wurde auch entdeckt, wie und in welcher Sequenz diese Verbindungen miteinander reagieren. Es waren die Pionierarbeiten für unser Verständnis, wie Energie biochemisch umgewandelt, gespeichert und für die Leistungen der Zelle in Form von ATP (bzw. GTP, CTP und UTP) zur Verfügung gestellt wird.
Bereits 1922 hatte Otto Meyerhof als Assistent am Physiologischen Institut der Universität Kiel gemeinsam mit A. V. Hill den Nobelpreis für Medizin für Forschungen zur Energieumwandlung im Muskel erhalten. Auch vier Mitarbeiter Meyerhofs aus dieser Zeit wurden später mit dem Nobelpreis ausgezeichnet: Fritz Lipmann für seine Entdeckungen zum Fettstoffwechsel (1953), Severo Ochoa für seine Beiträge zum genetischen Code und die Entdeckung der RNA-Polymerase (1959), André Lwoff für seine Arbeiten zur Genomorganisation in Bakterien (1965) und George Wald für seine Beiträge zur Molekularbiologie des Sehens (1967).
Diese frühen Arbeiten bezogen sich vor allem auf Stoffwechselvorgänge in der Zelle. Doch über die Speicherung unseres Erbmaterials in den Sequenzen der DNA und den riesigen Unterschied zwischen DNA und der aktiven RNA wußte man noch nicht viel. Das änderte sich erst mit der Entwicklung besserer Geräte und genauerer Untersuchungsmethoden.
Die Entdeckung der Energiefunktion des Adenosintriphosphats war sozusagen der erste Schritt in eine noch ungeahnte Richtung. Mehr und mehr entwickelte sich die Erkenntnis, daß praktisch alle Prozesse in der Zelle mit diesen Energieprozessen verbunden sind.
Heute weiß man auch sehr viel mehr über den Phosphatstoffwechsel in der Zelle: Alle Nukleosidtriphosphate der Bauteile der RNA und DNA – wie das Adenosintriphosphat, das Guanosintriphosphat (GTP), das Cytidintriphosphat (CTP) und das Uridintriphosphat (UTP) – sind energiereiche chemische Verbindungen, die wie eine universelle Energiewährung in der Zelle funktionieren. Sie versorgen fast jede Lebensfunktion mit Energie: die Bewegungen der Muskeln, die Aktivität des Herzens, die molekularen Ionenpumpen im Nervengewebe, den Stofftransport, die Proteinsynthese der RNA und bei Leuchtinsekten auch die Lichtproduktion.
Mit der Entdeckung der Doppelhelixstruktur der DNA 1953 wurde zum ersten Mal klar, daß biologische Informationen als linearer Code gespeichert und bei der Zellteilung verdoppelt werden. 1961 wurde dann die mRNA entdeckt, die bei den heutigen Covid-Impfungen eine entscheidende Rolle spielt.
Die Zelle als Maschinenraum
Um die durchschlagende Idee der mRNA-Impfstoffe zu verstehen, ist vor allem die hochspezialisierte Tätigkeit der Ribonukleinsäure bei der Proteinbiosynthese interessant, und dabei insbesondere die Rolle der mRNA. Bei diesem Biosynthesevorgang – erstens dem „Kopieren“ der Informationen von der DNA (der Transkription) und zweitens dem „Übersetzen“ der Informationen für ihre speziellen Aufgaben im Körper – gelangen alle wichtigen lebensnotwendigen Informationen, die in den von uns verspeisten Nahrungsmolekülen vorhanden sind, an „Ort und Stelle“ und ermöglichen es unserem gesamten Körper, zu funktionieren.
Beginnt man mit der Nahrungsaufnahme, so stellt sich die Frage: Wie kommen das Wurstbrötchen und seine Nahrungsmoleküle eigentlich in unsere Zellen? Wie kann unser Körper sie nutzen? Dabei fällt eines besonders auf: In den Zellen spielen beim Energiestoffwechsel Aminosäuren die Hauptrolle, die zu allen Arten von lebensnotwendigen Proteinen umgewandelt werden. Die Zellen brauchen daher dringend ständig neue Aminosäuren aus Proteinen, die man sogar als essentiell und nichtessentiell unterteilt hat. Die Erkenntnis der Bedeutung der Proteine für unser „ordentliches“ Funktionieren – unsere Gesundheit – hat sich erst in den letzten Jahrzehnten mit der Erforschung dieser Bauteile entwickelt.
Der Weg des Wurstbrötchens durch die Speiseröhre und den Magen läßt sich noch einfach nachvollziehen, obwohl schon im Mundraum verschiedenste chemische Verdauungsvorgänge mit der Nahrung beginnen. Wenn die Nahrung dann vom Magen weiterwandert und im Dünndarm zerlegt und mit allen möglichen Enzymen, Säuren, Basen etc. versetzt wird, dann bekommt man schon eine Ahnung davon, daß wir es in unserem Körper praktisch mit einem richtigen Chemiewerk zu tun haben (Abbildung 3).
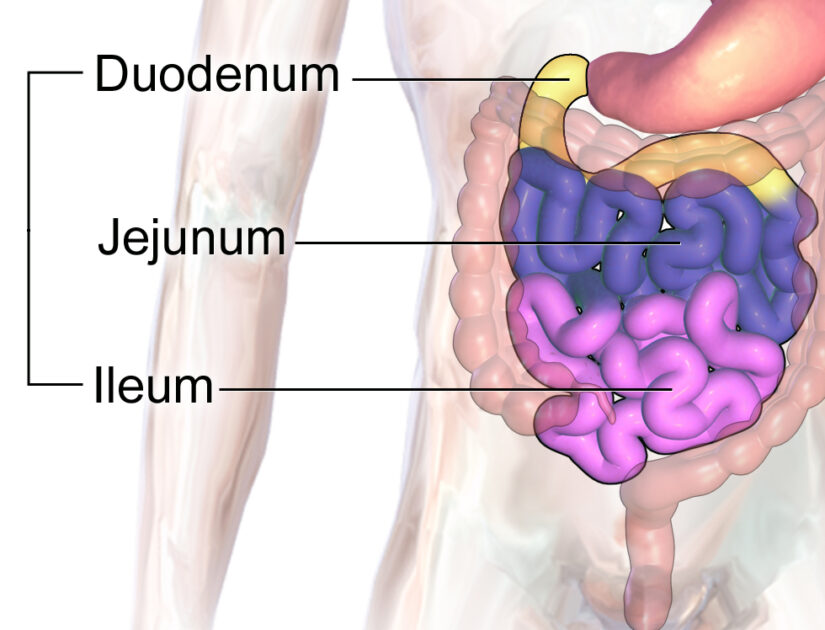
Im Dünndarm erkennt man das Wurstbrötchen schnell nicht mehr wieder; nach und nach werden alle seine Bestandteile bis auf einige unverdauliche Reste durch die Wände des Dünndarms – der mit all seinen Zotten und verzweigten Oberflächen immerhin 7 km lang ist – ins Blut und dann in die Zellen aufgenommen.
Giulia Enders beschreibt diesen Vorgang in ihrem Buch Darm mit Charme sehr anschaulich:
„Die allerletzte Verkleinerung der Nahrungsmittel, die wir zu uns nehmen, passiert letztendlich im Dünndarm. Ganz am Anfang gibt es ein kleines Loch in der Darmwand, das ist die Papille. Sie erinnert ein bißchen an die Speichelpünktchen im Mund – aber ist größer. Durch diese winzige Öffnung werden unsere Verdauungssäfte auf den Nahrungsbrei gespritzt. Sobald wir etwas essen, werden sie in der Leber und in der Bauchspeicheldrüse produziert und dann zur Papille geliefert. Sie enthalten die gleichen Bestandteile wie Waschmittel und Spüli aus dem Supermarkt: Verdauungsenzyme und Fettlöser. Waschmittel wirken gegen Flecken, weil sie fettige, eiweißhaltige und zuckrige Substanzen sozusagen von den Kleidern ,wegverdauen‘ und im Abwasser abtransportieren, während alles naß geknetet wird. Das ist so ziemlich das gleiche, was im Dünndarm passiert. Hier werden allerdings vergleichsweise riesige Stücke Eiweiß, Fett oder Kohlehydrate aufgelöst, um über die Darmwand in das Blut zu gelangen. Ein Apfelstückchen ist dann kein Apfelstückchen mehr, sondern eine Nährlösung aus Milliarden und Abermilliarden energiereichen Molekülen.“ (S. 48)
Die für unsere Körperzellen interessanten Aminosäuren (Abbildung 4) gelangen also über das Blut in die Zellen, wo dann unablässig die Proteinbiosynthese der RNA beginnt. Aus den Aminosäuren-Bausteinen werden zusammen mit der Geninformation, die sich die RNA von der DNA holt, genau die Proteinmoleküle hergestellt, die an den verschiedensten Stellen des Körpers benötigt werden. Zum Beispiel muß die Leber nach einigen Bierchen zuviel bestimmte Proteine einsetzen, um sich zu regenerieren, dann muß an einer Stelle am Finger, wo man sich geschnitten hat, zunächst ein Fremdkörper bekämpft und dann die Haut erneuert werden. Verschiedene Entzündungsprozesse, die im Körper entstanden sind, müssen abgewehrt, repariert und geheilt werden.

Jahrzehntelang hat man die Bedeutung der Ribonukleinsäure unterschätzt. Heute, nachdem man ihre Rolle beim Energiestoffwechsel der Zelle zusammen mit der Proteinbiosynthese und dem „Scannen“ der Erbinformationen entdeckt hat, läuft die Forschung auf Hochtouren. Jede Woche gibt es neue Erkenntnisse über wichtige RNA-„Schnipsel“ und deren Wirkungen. Wir wissen heute: die RNA kopiert längst nicht nur die im Zellkern gespeicherte Abfolge des Gencodes (der DNA) und transportiert die genetischen Daten in die verschiedenen Bereiche, sondern neuere Erkenntnisse deuten sogar darauf hin, daß manche RNA-Moleküle selbst die Kontrolle vieler Zellfunktionen übernehmen können. Ihr Einfluß geht so weit, daß sie während der Zellentwicklung einzelne Proteine an- und wieder ausschalten kann und damit über den Werdegang der gesamten Zelle entscheidet, sozusagen über Leben oder Absterben. Auf diese Weise entscheiden manche RNA-Schnipsel darüber, zu welcher Art von Gewebe Zellen heranwachsen, ob zu Schleimhautzellen im Darm oder Muskelgewebe im Herzen. Je mehr über die RNA herausgefunden wird, desto mehr erkennen die Forscher, was die RNA in Wirklichkeit alles kann. Ohne sie gibt es kein Leben, keine Muskelaktivität, keinen Herzschlag.
Bei der Proteinsynthese wird durch Enzyme (die Polymerasen) und Katalysatoren die Synthese von neuen Ribonukleinsäure-Molekülen an der DNA abgelesen bzw. „gescannt“. Grundsätzlich finden bei diesem Vorgang zwei Hauptprozesse statt: die Transkription und die Translation. Zunächst werden die für den Proteinaufbau benötigten Gene der DNA-Basen von einem Enzym während der Transkription abgelesen und kopiert, und zwar immer ein kleines Stück „Info“ der DNA, ein „Codon“. Diese Informationen werden wie nach einem Bauplan abgelesen und ein passendes Stückchen mRNA-Sequenz komplementär gebildet. Das ganze geht in drei Schritten vor sich: Initiation, Elongation und Termination.
Die Initiation beginnt damit, daß sich das Enzym RNA-Polymerase an einer spezifischen Basenabfolge, der sogenannten Promoterregion, am Codon (einem kurzen Stückchen) des DNA-Strangs festsetzt. Dies dient sozusagen als Starter.
Der zweite Prozeß ist die Elongation, bei der die Polymerase am Codon der DNA entlangläuft und bei der sie die Wasserstoffbrückenbindungen zwischen den einzelnen Basenpaaren auflöst. Sie „kopiert“ oder „scannt“ dieses Stück und setzt gleichzeitig einen komplementären RNA-Strang aus RNA-Nukleotiden zusammen. Dies ist nun die sogenannte Boten- oder Messenger-RNA (mRNA). Der einzige Unterschied des neuentstandenen Codons ist, daß hier statt der Base Thymin das Uracil verwendet wird.
Der dritte Teil des Prozesses ist nun die Termination, d.h. sobald ein neues Codon (Erbinformation auf der DNA) beginnt, endet der Transkriptionsvorgang, so daß sich die RNA-Polymerase und die hergestellte mRNA von der DNA lösen.
Nun beginnt der nächste wichtige Schritt der Proteinbiosynthese, die Translation. Dabei handelt es sich – einfach ausgedrückt – darum, die spezifischen Aminosäuresequenzen zu bilden und daraus Proteine für die verschiedensten Regionen des Körpers herzustellen.
Im Vorfeld binden sich wiederum neue Teile der RNA, nämlich Transfer-RNAs (tRNAs) an eine spezifische Aminosäure (Abbildung 5).
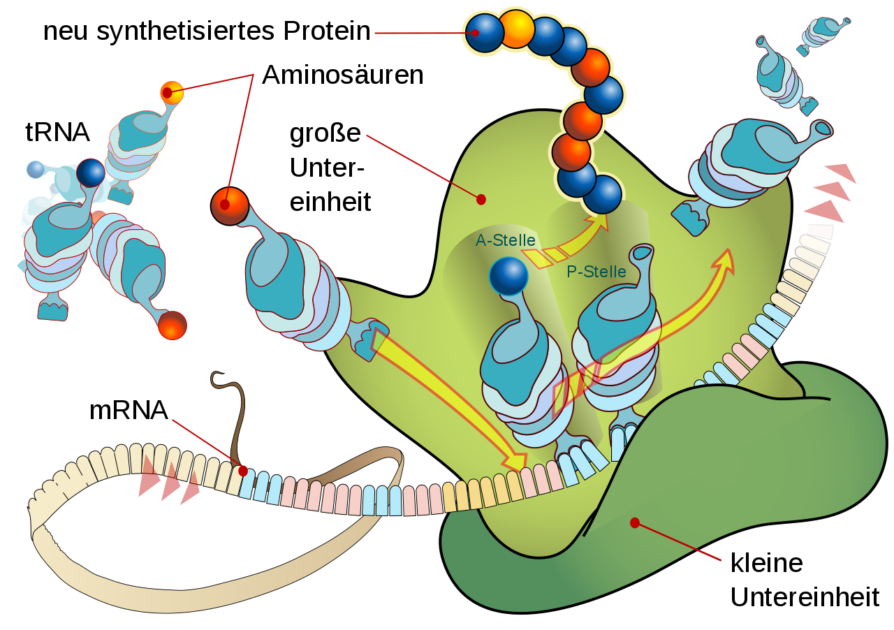
An der Proteinbiosynthese und den Vorgängen in der Zelle wird weiter intensiv geforscht, und es gelingt, immer mehr dieser komplexen Aufgaben der RNA zu entschlüsseln. Ein bedeutender erster Schritt war, die Rolle der mRNA aufzuklären und darüber hinaus, diese Prozesse zu benutzen, um auch „fremde“ Informationen an Zellen und damit Organe weitergeben zu können, Aufgaben wie zum Beispiel, die Vermehrung von Viren zu verhindern. Ein nächster weiterer Schritt wird nun sein, den Prozeß auch gegen Krebszellen zu richten und damit ihr Wachstum zu stoppen. Mit diesen und vielen weiteren Projekten sind Forschergruppen weltweit bereits erfolgreich. Die Covid-19-Impfforschung hat dazu beigetragen, daß nun die Bedeutung der Biochemie für die Bekämpfung von Krankheiten viel umfassender erkannt wird.
Wie funktioniert ein mRNA-Impfstoff?
Die Proteinbiosynthese zu benutzen, um Fremdkörper in der Zelle auszuschalten, ist eine geniale Idee – das Produkt der langjährigen Geschichte biochemischer Erforschung des oben beschriebenen Energiestoffwechsels der Zelle und ihrer Aufgabe, stets die „richtigen“ Informationen, welche in den DNA-Nukleid-Codons festgelegt sind, für alle Bereiche des Körpers zu produzieren. Um einen Impfstoff zu entwickeln, ging es darum, diesen Mechanismus zu benutzen, um Informationen gegen Viren im Körper zu verbreiten.
Ein RNA-Impfstoff besteht also aus synthetisch hergestellter mRNA, die bei der oben beschriebenen Transkription ein Oberflächenprotein des Virus mittels der Proteinbiosynthese produziert. Dieses Oberflächenprotein wurde aber bei der Entwicklung des Impfstoffs so ausgewählt, daß es vom körpereigenen Immunsystem als Fremdkörper erkannt wird.
Bei der Herstellung eines solchen mRNA-Nukleids trat lange das Problem auf, daß es sehr instabil war. Das wurde dadurch gelöst, daß man die Information in ein Lipid-Nanopartikel (also Fett) verpackt hat, so daß die Impfstoff-RNA tatsächlich von Zellen der geimpften Personen aufgenommen wird. Sobald die mRNA in die Zelle des Impflings gelangt ist, setzt sie eine Translation in Gang, welche nun das gewünschte Proteinteilchen des Virus und die dagegen gerichtete Immunreaktion erzeugt; die als Bote benutzte, synthetisch hergestellte mRNA des Impfstoffes selbst wird nach einiger Zeit in der Zelle wieder abgebaut.
Eine ganz wichtige Tatsache dabei ist, daß ein solcher mRNA-Impfstoff gegen alle proteinbasierten Antigene entwickelt werden kann, so auch z.B. gegen Grippeviren oder Krebszellen.
Nach dem Auftreten des SARS-CoV-2-Virus wurde diese geniale Idee vorangetrieben, weil plötzlich auch genügend Forschungsgelder bereit standen, um einen Impfstoff zu entwickeln. Seitdem ist die Biochemie und vor allem die weitere Erforschung der RNA sowie der vielen Vorgänge im Energiestoffwechsel der Zelle ein boomender Bereich. Besonders für die Krebsbekämpfung verspricht dieser Forschungsbereich große Fortschritte.
Es gibt bereits Forschungsprojekte gegen mehrere Viren, wie zum Beispiel HIV, Tollwut, Zika, Chikungunya, natürlich alle Variationen der Grippe und das Dengue-Fieber und Malaria.
Riesenschritte zur Bekämpfung von Krebs und gefährlichen Viren
In China gab es schon im Februar 2021 einen Durchbruch in der Forschung an mRNA-Impfstoffen gegen Krebszellen. Der entwickelte Wirkstoff konnte im Labortest das Immunsystem so umprogrammieren, daß Krebszellen schrumpften und der Krebs an der Ausbreitung gehindert wurde. Chinesische Forscher vom Chinese National Centre for Nanoscience and Technology in Beijing konnten außerdem erfolgreich einen Impfstoff entwickeln, der ein spezifisches Protein von Tumorzellen bekämpft.
Die Herausforderung dabei war genauso wie bei der Entwicklung des Covid-19-Impfstoffes, daß nämlich die mRNA-Moleküle sehr instabil sind und von den Enzymen schnell wieder abgebaut werden. Die Biochemiker Guangjun Nie, Hai Wang und ihre Mitarbeiter fanden dann eine Lösung: Sie kombinierten ein Hydrogel mit Ovalbumin-mRNA, einem in Hühnerei vorkommenden Protein. In den Versuchen an Mäusen mit Melanom konnte die so hergestellte mRNA mindestens einen Monat lang wirken. Im Gegensatz zu nichtbehandelten Mäusen konnte der Krebs sich nicht weiter ausweiten oder die Lungen befallen. Guang Nien betonte, die Hydrogel-mRNA habe ein großes Potential, mit nur einer Behandlung eine langanhaltende Immunantwort gegen Krebszellen zu erreichen.
Die Mainzer Firma BionTech hat im Juni 2021 eine Phase-2-Studie zur Behandlung von fortgeschrittenem Hautkrebs begonnen.
Am MD Anderson Cancer Center der University of Texas in Houston arbeiten die Wissenschaftler ebenfalls an der Entwicklung von mRNA-Impfstoffen gegen Krebs. Alle Forscher sind sich einig: Das größte Problem von Krebs ist, daß der Körper die Krebszellen nicht selbständig erkennt, weshalb das Immunsystem keine Antikörper gegen die Krebszellen bilden kann. Van Morris, Assistenzprofessor für Magen-Darm-Krebsmedizin in Houston, erläuterte gegenüber der Zeitschrift National Geographic:
„Einer der großen Vorteile der mRNA-Technologie ist, daß sie unabhängig von der Krebsart eingesetzt werden kann. Ob es sich um Brust- oder Lungenkrebs handelt, ist unerheblich, solange es möglich ist, die Mutationen zu identifizieren“.
mRNA-Impfstoffe könnten demnach auf Patienten maßgeschneidert werden, so daß der Körper eigene Krebsproteine herstellen kann, die dem Immunsystem anzeigen, gegen was er ankämpfen muß. Die eingeimpfte mRNA würde alle ähnlichen Krebszellen bekämpfen.
Im Bereich der traditionellen chinesischen Medizin, die seit über 2000 Jahren auf die Heilkraft der Pflanzen setzt, wurde jüngst ein hochinteressanter Beweis für die Wirkung bestimmter Kräuter erbracht. Ein Forscherteam um Prof. Chen Yu Zhang an der Universität Nanjing untersuchte die Wirkung chinesischer Grippemittel (also Kräutermischungen aus der Traditionellen Chinesischen Medizin TCM) im Blut. Zu ihrer Überraschung fanden die Wissenschaftler aber nicht nur Erbgutteile (Mikro-RNA) der gesuchten Kräuter, sondern auch die RNA von 30 verschiedenen Gemüsepflanzen. Bisher war man davon ausgegangen, daß die Bestandteile unserer Nahrung komplett durch die Magensäure zerstört werden. Daher war es eine Sensation, daß Pflanzen-RNA im menschlichen Körper die Produktion wichtiger Proteine beeinflußt und damit unsere Gene. Erste deutsche Labore haben bereits eigene Forschungsanträge zur Untersuchung dieser Effekte gestellt. Hier entsteht eine ganz neue Fachdisziplin, die Epigenetik, die auch die Steuerung von Genen durch die Nahrung untersucht.
Die jetzt überall auf der Welt angelaufene Forschung ist mit großer Hoffnung verbunden. Der Erfolg des Einsatzes von mRNA gegen bisher unheilbare Krankheiten wäre ein Riesenschritt in der Medizin und ein großer Schritt für das menschliche Überleben.
Literaturverzeichnis
- Biography of Otto Fritz Meyerhof http://www.nobel.se/medicine/laureates/1922/meyerhof-bio.html Eckart, W. U. (1995)
- A History of the Max-Planck-Institute for Medical Research; Otto Meyerhof and the Physiology Department: The Birth of Modern Biochemistry states@mpimf-Heidelberg.mpg.de
- Arbeitskreis Geschichte der Biochemie https://gbm-online.de/geschichte-der-biochemie.html
- Giulia Enders: „Darm mit Charme“, 2015
- Manfred Schartl, Manfred Gessler, Arnold von Eckardstein: Biochemie und Molekularbiologie des Menschen. Elsevier: München 2009
- https://www.desy.de/forschung/anlagen__projekte/european_xfel/index_ger.html
- https://www.op-online.de/region/darmstadt/krebs-forschung-behandlung-methode-heilbar-impfung-mrna-corona-zr-90890526.html
